Kovy
25.10.2013 21:29
- Prvek je tím kovovější, čím méně se jeho el. konfigurace liší od el. konfigurace předchozího vz. plynu. A čím menší je jeho ionizační E.
- Typickými kovy z chemického hlediska jsou alkalické kovy (Li, Na, K, Rb, Cs, Fr)
- Ionizační E (I) je E, které je potřeba k odtržení 1 e- od izolovaného atomu plynu.
- Mg - má 2e- ve valenční vrstvě - ty jdou "odtrhnout" snadno, ale už ten třetí se odděluje těžko, protože je v hlubší vrstvě.
- Nejtěžší kovy v VIII.B skupině - osmium, iridium, platina
- Známe tzv. triády kovů
- Na má menší hustotu než voda (viděli jsme s Bohmovou pokus) a tak i další kovy
- Ušlechtilé kovy by neměly měnit svůj vzhled v přítomnosti kyslíku - na vzduchu.
- Obecné kovy s kyslíkem reagují (Al+O 2 --- Al 2 O3)
- Pasivace - kov se pokryje vrstvičkou oxidu a tak zabráňuje další korozi
- Kovy buď mají nebo nemají schopnost se pasivovat.
- Proti korozi kovy chráníme:
- nátěry z pigmentů, olejů
- pozinkováním, pochromováním, pocínováním
- fosfatací
- Kovy jsou lesklé, tažné a kujné, dobré vodiče tepla a elektřiny, šedostříbrolesklé, schopné vytvářet slitiny
- elektrická vodivost s rostoucí teplotou klesá
Kovová vazba
- kationty libovolného kovu jsou rozmístěny do uzlových bodů krystalové mřížky. Valenční elektrony se mezi nimi volně pohybují. - malý počet valenčních elektronů.
krychlová:

šesterečná:
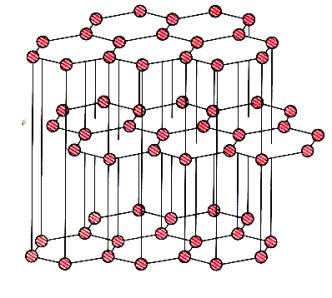
Slitiny
- je to homogenní směs
- Má lepší vlastnosti než samotný kov - proto se vyrábí: větší tvrdost, tažnost, odolnost, jiné teploty tání a varu
- příklady slitin:
- bronz: Cu + Sn
- mosaz: Cu + Zn
- dural: Al + Mn + Cu + Mg
- konstantan: Ni + Mn + Cu
- 14-karátové Au - 585/1000 = 58,5% Au + Ag + Cu + Ni + Cr
- 18-karátové Au - 750/1000 = 75% Au ...
- amalgámy: Hg + kov (Au, Sn, Ag, Pb)
- zubní amalgám: Hg 50% + Ag + Cu + Sn
Chemické vlastnosti kovů
- Závisí na tom, kde je prvek postaven v Beketovově řadě kovů v elektrochemické řadě napětí

- (https://www.zschemie.euweb.cz/redox/rada.gif)
- Kov umístěný vlevo, je schopen vytěsnit kov umístěný od něj vpravo z roztoku jeho soli.
Reakce:
- Zn + CuSO4 ---- Cu + ZnSO4 (měď se síranem spolu dál nereagují) (plíšek ze zinku by na svém povrchu vytvářel měď)
(https://www.sciencephoto.com/image/4067/530wm/A5000102-Displacement_reaction%2C_Zn_in_CuSO4_solution-SPL.jpg):
- 2Na + 2H2O --- 2NaOH + H2 (bouřlivá reakce)

- Zn + 2 HCl --- ZnCl 2 + H 2
- Cu + HNO 3 --- Cu(NO 3 ) 2 + NO ( nebo NO 2 ) + H2O (vznik oxidu)

(https://genchem.rutgers.edu/cudisolv.jpg)
- 2Al + 6 HCl --- 3H 2 + 2AlCl 3
- Mg + Pb(NO 3 ) 2 --- Mg( NO3 ) 2 + Pb
- Fe + AlCl 3 --- neprobíhá
- Cu + 2H 2 SO4 --- CuS O 4 + 2H2O + SO2 (vznik ox idu)
- lučavka královská - (královská voda) rozežere i zlato - je to nevětší známá žíravina: HNO3 + HCl = 1:3
Ája